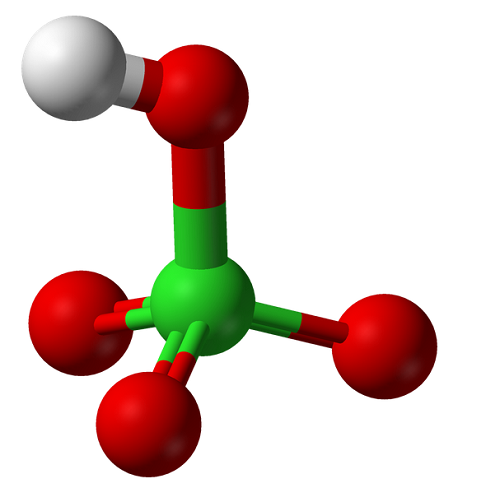
El ácido perclórico es un compuesto inorgánico, que suele encontrarse en forma de solución acuosa. Este compuesto incoloro es un ácido fuerte comparable en fuerza al ácido sulfúrico y al ácido nítrico.
Es un oxidante poderoso, pero sus soluciones acuosas de hasta el 70% son notablemente inertes, mostrando sólo propiedades de ácido fuerte y ninguna otra propiedad oxidante. Por encima de concentraciones del 70% la velocidad de las reacciones oxidantes aumenta rápidamente con el aumento de la concentración de ácido.
Uno de los principales usos del perclórico es para la preparación de sales de perclorato, principalmente el perclorato de amonio (un combustible para cohetes muy importante). Sin embargo, también es bastante corrosivo e inflamable al mezclarse con ciertos compuestos, por lo que se considera peligroso.

El ácido perclórico en la cohetería
Como ya se mencionó, el perclorato de amonio es un combustible para cohetes de importancia crucial en la industria aeroespacial. Con el crecimiento de la cohetería en los últimos años, esa importancia se ha disparado, provocando un aumento considerable de la producción de ácido perclórico a nivel mundial.
De hecho, se producen millones de kilogramos del ácido cada año. Un detalle curioso considerando lo altamente peligroso que puede llegar a ser dado lo volátiles que resultan sus sales. Aunque es también el preferido por diversos químicos para realizar síntesis de compuestos.
Toxicidad
El ácido perclórico es capaz de causar quemaduras en las vías digestivas, respiratorias, quemaduras en los ojos y en la piel. Así mismo, es considerado como un fuerte oxidante, hasta el punto de que el contacto con otros materiales puede causar un incendio. Incluso el calentamiento puede causar una explosión.
Además de ser un líquido corrosivo, aunque no es combustible, en algunas circunstancias el ácido perclórico puede actuar como oxidante y presentar un riesgo de explosión. Los cristales perclóricos, o el ácido perclórico en forma cristalina, es un compuesto inorgánico extremadamente peligroso.
Los cristales se forman a veces debido a la condensación dentro de las campanas de ventilación de los laboratorios químicos o en botellas almacenadas durante largos períodos en el laboratorio.
Entre los principales peligros se encuentra el que los cristales de perclorita estén sujetos a la explosión en el momento del impacto. Los materiales orgánicos son especialmente susceptibles a la combustión espontánea si se mezclan o entran en contacto con el ácido perclórico.
En algunas circunstancias, los vapores de ácido perclórico forman percloratos (en los conductos de las guanteras) que son sensibles a los choques.